在研产品管线
在研产品管线
靶点 (药物类型)












临床
临床
临床





- 单药 (CLINCH)



- 联合JS207 [PD-1 x VEGF双特异性抗体]

- 单药 (PROBE)

- 单药 (PERFORM)


- 药物发现
靶点 (药物类型)










临床
临床
临床
申请

- 联合地塞米松 (MARCH)

- 联合硼替佐米,地塞米松 (BENCH)

- 单药 (SEARCH)*


- 联合 R-GDP (DLBCL-030)


- 联合芦可替尼 (MF-034)


- 单药 (EC-042)

- 联合特瑞普利单抗 (TORCH-2)**
 AnTenGager® TCE 2.0
AnTenGager® TCE 2.0
新型第二代 “2+1” TCE 平台,采用空间位阻遮蔽技术,可广泛适用于多种实体瘤、血液瘤或自身免疫性疾病。
-
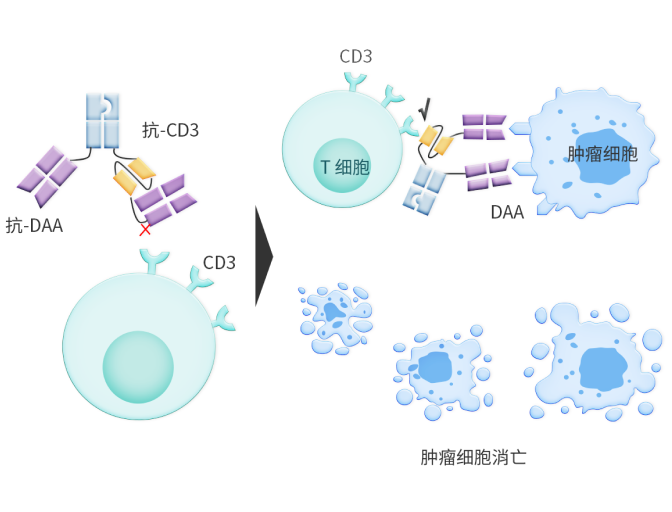 AnTenGager® 机理
AnTenGager® 机理
-
 AnTenGager® 独有的靶向全新构象表位的CD3抗体
AnTenGager® 独有的靶向全新构象表位的CD3抗体
T细胞衔接器(TCE)已在血液系统肿瘤的治疗中显示良好疗效,并在近期开始显示出治疗实体瘤的潜力。但由于不理想的疗效和较高的CRS风险,TCE在实体瘤治疗中的应用仍非常有限。
德琪医药的新型“2+1”TCE技术平台AnTenGager<sup>®</sup> 可以有效克服这些问题,因为它可通过诱导疾病相关抗原(DAA)依赖的T细胞结合和激活,在实现较强的活性的同时降低发生CRS的风险。
它可实现与DAA(包括表达水平较低的DAA)的二价结合,同时使用了由德琪医药自主研发的可靶向作用于一个特殊构象表位的CD3抗体序列。它利用长度优化过的连接子将一个CD3单链抗体(scFv)结合至TAA抗体铰链区,这让起初被Fab抗体臂掩盖的CD3结合域仅在DAA交联条件下暴露,进而实现T细胞的条件性激活。
优势
-
 创新性
创新性

自主开发的CD3序列可与CD3的特殊表位结合
-
 空间位阻遮蔽
空间位阻遮蔽

只在疾病相关抗原(DAA)交联条件下结合并激活T细胞
-
 安全有效
安全有效

降低出现细胞因子释放综合征和"弯钩效应"的风险并增强疗效
-
 可成药性
可成药性

较高的可开发性
开放合作
德琪医药现已面向行业伙伴开放基于AnTenGager® TCE 2.0的合作,包含以下三种合作方式:✓ 共同发现/开发新型TCE
以创新构想为起点,与您携手从零构建,共同打造创新TCE疗法
✓ 自带抗体合作
如您已拥有针对特定DAA的抗体,可利用我们的平台快速生成并优化新型TCE
✓ 授权现有候选药物
获取并推进我们已验证的候选TCE药物,加速您的开发进程
如果您有兴趣与德琪医药合作,请联系: bd@antengene.com
在研AnTenGager®管线
评估
(IND)










发现
评估
评估
评估